曲靖市2014年招聘教师初中化学考试大纲
2014-05-20来源:曲靖市教育局
化 学
2014年曲靖市教育系统公开招聘教师考试
专业知识 教法技能 大纲
化 学(初中教育岗位)
曲靖市教育局
一、考试性质
曲靖市教育系统公开招聘教师考试属选拔性考试。教育行政部门根据教育事业改革和发展的需要,考查、考核考生从事教师工作的专业知识、教育教学能力,按招考录用计划择优录用。因此,考试具有较高的信度、效度、区分度和一定的难度。
二、考试形式与试卷结构
考试形式:闭卷,笔试。“专业知识”满分100分,考试用时100分钟;“教法技能”满分50分,考试用时50分钟;二者合卷满分共150分,考试限定用时150分钟。
试题类型:“专业知识”的题型为单项选择题、填空题、简答题、推导题、计算题;“教法技能”的题型为单项选择题、填空题、简述题、教学设计题。
三、考试内容
专业知识
以现行大学师范类化学教育专业主干课程《无机化学》、《有机化学》和《义务教育化学课程标准》、《中学化学教学法》为依据,综合高、初中知识,突出大学专科师范类化学教育专业上述主干课程的主要内容,以初中化学教师应具备的教育教学水平和能力要求为重点确定考试内容。
无机化学部分
1.一些化学基本概念和定律
(1)化学有关基本概念(原子、分子、元素、核素、同位素、相对原子质量……)等;
(2)“物质的量”及其单位——摩尔的概念及计算;
(3)理想气体状态方程及应用条件;
(4)分压定律及有关概念。
2.化学平衡
(1)化学平衡的概念,平衡常数及意义;
(2)多重平衡规则;
(3)有关化学平衡的计算;
(4)化学平衡移动原理。
3.电离平衡
(1)酸碱电离理论和酸碱质子理论;
(2)PH的意义及PH与氢离子浓度的相互换算;
(3)同离子效应,盐效应;
(4)缓冲溶液的组成、原理及计算;
(5)Ksp的意义及溶度积规则:溶度积Ksp与摩尔溶解度(S)的关系、换算及Ksp有关计算。
4.化学反应速度
(1)化学反应速度及表示方法;
(2)两种反应速度理论——碰撞理论和过渡状态理论及应用。
5.化学热力学初步
(1)状态函数U、H、S、G、△U、△S、△H、△G、△ƒHo、△ƒGo和So的概念、意义和性质;
(2)热力学第一定律和盖斯定律及计算;用△ƒHo、△ƒGo和So求算标准状态和非标准状态下体系的△Ho、△So和△Go(△G);
(3)吉布斯一赫姆霍兹公式及意义;
(4)吉布斯一赫姆霍兹公式的计算和应用;
(5)化学反应等温式及公式 △Go=–TRlnK 的应用。
6.原子结构和元素周期系
(1)原子结构有关术语和概念;
(2)四个量子数n、l、m、ms的意义、取值和相互关系;
(3)用四个量子数写出1—4周期常见元素的电子结构式,由结构式确定元素所在周期、族、区、特征电子构型(即价电子构型)和元素名称。
(4)原子结构与周期系的关系。
7.分子结构和晶体结构
(1)化学键参数有关基本概念和分子的性质(极性、磁性);
(2)离子键和共价键的基本特性及其区别;
(3)共价键理论、杂化轨道理论;
(4)分子间力和氢键;
(5)晶体的四种基本类型和特点。
8.氧化还原反应
(1)氧化还原有关基本概念和方程式配平(包括氧化数法—离子~电子法)。
(2)电极电势(φ0)的意义,用φ0判断氧化剂、还原剂的强弱,选择适当的氧化、还原剂;
(3)用φ0计算并判断氧化还原反应的方向和程度;(公式 );
);
(4)标准元素电势图及应用。
9.配位化合物
(1)配合物有关基本概念;
(2)配合物的命名;
(3)用杂化轨道理论讨论常见配合物的杂化类型及对其性质的影响;
(4)配合物稳定常数(K稳)的意义及应用。
10.元素部分
(1)主族元素、副族元素的特性;
(2)金属通性,元素之最(例如:最轻的气体、地壳中含量最高的元素,比重最大的金属,硬度最大的金属……);
(3)常见元素卤素、氧、硫、氮、磷、碳、硅、硼、铝、铜、银、锌、汞、铬、锰、铁、钴、镍单质及重要化合物的结构和性质;
(4)“缺电子原子”、“等电子原子”、“缺电子化合物”、“等电子体”、“惰性电子对效应”等基本概念及实例;
(5)常见无机物的结构、性质及常见化学试剂的俗名。
有机化学部分
1.烷烃:掌握有机化合物的分类、命名原则;理解б键的定义及特点;了解烷烃构型、物理性质及变化规律;掌握卤代反应—游离基反应的基本历程;了解烷的氧化、裂解反应。
2.烯烃:熟练掌握烯烃的系统命名法、Z/E、顺/反命名法;理解sp2杂化及п键定义、特点;认识加成反应特点,理解离子型亲电加成反应;掌握马氏规则及过氧化物效应;掌握烯烃的鉴别方法。
3.炔烃 二烯烃:掌握炔烃、二烯烃的命名方法,sp杂化特点;掌握炔烃的性质(加成、聚合、氧化);掌握共轭二烯烃的结构特点及重要性质;掌握炔烃的鉴别方法;了解共轭效应。
4.脂环烃:熟练掌握脂环烃命名方法;掌握环烷烃的结构特点;掌握环烷烃性质特别是小环烷烃的性质。
5.芳烃:熟练掌握芳烃的命名方法;理解苯环结构、特征;掌握苯及同系物的化学性质;了解亲电取代反应历程;掌握定位规则、定位规则的应用;掌握芳烃的鉴别方法。
6.多环芳烃和非苯芳烃:了解联苯的命名及性质;理解非苯芳烃的概念及休克尔规则。
7.立体化学:掌握立体异构、光学异构、对称因素、手性碳、对映体、非对映体;掌握Fischer投影式书写方法和R、S命名法。
8.卤代烃:熟练掌握卤代烃的化学性质及结构与性质间关系;了解亲核取代反应历程、消除反应历程;掌握卤代烃的制备方法。
9.醇和醚:掌握醇、醚的命名、结构特点及化学性质的差异;掌握醇、醚的基本反应与鉴别方法;熟悉主要的醇、醚的制备方法。
10.酚:掌握酚的结构、命名及制法;掌握酚的化学性质及酚的鉴别方法。
11.醛和酮:掌握碳氧双键和碳碳双键的结构差异及在加成反应方面的异同;熟练掌握醛、酮的化学性质,重点是亲核加成反应,理解其反应历程;掌握醛、酮在化学性质上的差异,如氧化还原反应及歧化反应;掌握醛酮的鉴别方法。
12.羧酸及其衍生物:掌握羧酸及羧酸衍生物的系统命名法及常见羧酸的俗名;熟练掌握羧酸的化学性质;掌握诱导效应和共轭效应对羧酸性质的影响;了解羧酸及羧酸衍生物的制备方法;掌握羧酸衍生物的化学性质及它们之间的相互转化关系;熟练掌握丙二酸酯、乙酰乙酸乙酯在合成上的应用。
13.硝基化合物和胺:了解硝基化合物的结构、性质;掌握胺的分类、命名、结构;掌握胺的性质及碱性强弱顺序;了解区别伯、仲、叔胺的方法及重要的胺;掌握重氮盐的反应和偶合反应在有机合成中的应用。
14.重氮化合物和偶氮化合物:掌握重氮化反应;掌握重氮盐性质及其在合成中的应用。
15.杂环化合物:掌握杂环化合物的分类、命名;理解杂环化合物的结构与芳香性。
教法技能(化学教学)
1.《义务教育化学课程标准(2011年版)》:初中化学课程性质,课程基本观念,课程设计思路。
2.《义务教育化学课程标准(2011年版)》三维目标:知识与技能,过程与方法,情感态度与价值观。
3.《义务教育化学课程标准(2011年版)》内容标准:五个一级主题与每一级主题的若干个二级主题及其学习要求。
4.《义务教育化学课程标准(2011年版)》实施建议:教学建议与评价建议,明确教师不仅是知识的传授者,还是学生学习的引导者、组织者和合作者,以学生为主体、教师为主导制定教和学的计划,重视科学研究的教学,帮助学生尽快进入自主学习的轨道,保护学生学习兴趣,探究因人而异的教学方法。
5.化学教学的基本功和必备的能力:组织教材的基本功、设计实验和组织学生实验的基本功;应用化学知识解决实际问题的能力、驾驭课堂的能力、化学教学评价命题的能力、参与化学教学研究的能力。
6.制定学年(期)、单元、章节、课时教学计划,依据教学内容和学生实际备课、上课、辅导、批改作业、学生成绩考核,进行教学设计,编写教案、学案、说课案。
四、考试要求
专业知识
无机化学部分
1.一些化学基本概念和定律
(1)了解本章有关化学基本概念(原子、分子、元素、核素、同位素、相对原子质量……);
(2)掌握“物质的量”的意义及其单位—摩尔的概念,能熟练应用并进行有关计算;
(3)掌握理想气体状态方程及应用条件;
(4)了解分压定律及有关概念。
2.化学平衡
(1)掌握化学平衡的概念,理解平衡常数及意义;
(2)掌握多重平衡规则;
(3)掌握有关化学平衡的计算;
(4)熟悉化学平衡移动原理。
3.电离平衡
(1)了解酸碱理论的发展概况,掌握酸碱电离和酸碱质子理论;
(2)掌握PH的意义、PH与氢离子浓度的相互换算;
(3)掌握同离子效应,盐效应的概念及应用;
(4)了解缓冲溶液的组成、原理,掌握缓冲溶液PH值的计算;
(5)掌握Ksp的意义及溶度积规则:掌握Ksp与摩尔溶解度(S)的关系、换算及Ksp有关计算。
4.化学反应速度
(1)掌握化学反应速度的表示方法;
(2)会用活化分子、活化能(Ea)概念解释T、C(P)和催化剂对反应速度的影响。
5.化学热力学初步
(1)掌握状态函数 U、H、S、G、△U、△S、△H、△G、△ƒHo、△ƒGo和So的概念和性质;
(2)掌握热力学第一律和盖斯定律及计算;掌握用△ƒHo、△ƒGo和So求算标准状态和非标准状态下体系的△Ho、△So和△Go(△G)的方法;
(3)掌握吉布斯一赫姆霍兹公式及意义,掌握△G与△H和△S的关系,并会用于分析温度对化学反应自发性的影响;
(4)掌握吉布斯一赫姆霍兹公式的计算和应用,会用其判断反应自发进行的方向、程度;
(5)了解化学反应等温式的意义和用途,会用公式:△Go=–TRlnK 求算反应的△G和K(平衡常数)。
6.原子结构和元素周期系
(1)了解原子结构有关术语和概念;
(2)掌握四个量子数n、l、m、ms的意义、取值和相互关系;
(3)会用四个量子数写出1—4周期常见元素的电子结构式,并会由结构式确定元素所在周期、族、区、特征电子构型(即价电子构型)和元素名称;
(4)掌握原子结构与周期系的关系。
7.分子结构和晶体结构
(1)了解化学键参数有关基本概念和分子的性质;
(2)会根据化学键和分子结构判断分子是否有极性;
(3)掌握离子键和共价键的基本特性以及它们的区别;
(4)掌握共价键理论、杂化轨道理论, 会用上述理论确定常见共价小分子的杂化类型和基本性质;
(5)掌握分子间力和氢键的概念和应用;
(6)掌握晶体的四种基本类型和特点。
8.氧化还原反应
(1)掌握氧化还原有关基本概念和方程式配平(包括氧化数法—离子~电子法);
(2)理解电极电势(φ0)的意义,会用φ0判断氧化剂、还原剂的强弱,选择适当的氧化、还原剂;
(3)掌握用φ0计算并判断氧化还原反应方向和程度的方法;(公式 );
);
(4)掌握用准标元素电势图判断歧化反应及其反应程度的计算。
9.配位化合物
(1)了解配合物有关基本概念;
(2)掌握配合物的命名;
(3)掌握用杂化轨道理论判断常见配合物杂化类型、分子构型的方法;
(4)理解配合物稳定常数(K稳)的意义,掌握应用K稳计算并判断配位离解反应方向、限度,配离子生成和破坏的方法。
10.元素部分
(1)掌握主族元素、副族元素的特性;
(2)了解金属通性,掌握元素之最(例如:最轻的气体、地壳中含量最高的元素,比重最大的金属,硬度最大的金属……);
(3)掌握常见元素卤素、氧、硫、氮、磷、碳、硅、硼、铝、铜、银、金、锌、汞、铬、锰、铁、钴、镍单质及重要化合物的结构和性质;
(4)掌握“缺电子原子”、“等电子原子”、“缺电子化合物”、“等电子体”、“惰性电子对效应”等基本概念及实例;
(5)了解常见无机物的结构、性质,掌握常见化学试剂的俗名。
有机化学部分
1.考核学生掌握有机化合物的命名、主要性质、有机化合物的主要合成方法;
2.考察学生应用有机分子基本反应类型及主要官能团的特性和相互转化规律的能力。
教法技能(化学教学)
1.了解《义务教育化学课程标准(2011年版)》的课程性质、课程基本理念、设计思路、课程目标及内容标准。
2.了解《义务教育化学课程标准(2011年版)》的主要内容,明确化学教学在义务教育中的地位和作用,明确各部分内容的学习要求。
3.掌握化学教学的基本原则和方法。
4.能够创设情景激发学生的学习兴趣,把握好课堂教学结构,选择适当的教学方法进行教学设计,进行实际教学。
5.掌握科学探究和化学实验能力的要求,明确科学探究要素。
6.依据《化学课程标准》、教学内容和教学要求正确科学地评价学生成绩,指导学生学习,促进学生发展。
五、题型示例
专业知识
无机化学部分
一、单选题
1.根据酸碱质子理论,HNO3 + H2SO4 H2NO3 + H SO4- ,正反应中的酸是( )
H2NO3 + H SO4- ,正反应中的酸是( )
A.HSO4- B.HNO3 C.H2SO4 D.H2NO3=+
2.难溶电解质M2X的摩尔溶解度s与溶度积Ksp之间的定量关系式为( )
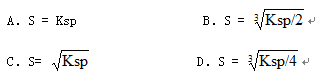
3.关于催化剂的下列说法中,正确的是( )
A.改变反应的热效应
B.改变平衡混合物的组成
C.不能使热力学上认为不能发生的反应发生
D.加快正反应速度,减慢逆反应速度
4.下列电子的量子数(n、l、m和ms)不合理的是( )

5.下列分子或离子中,键角最大的是( )
A.XeF2 B.NCl3 C.CO3=2- D.PCl4+
6.下列各对物质中,属于等电子体的是( )
A.O22- 和O3 B.C和B+
C.He和Li D.N2和CO
7.在Cr2O72-+I‑+H+→Cr3++I2+H2O反应式中,配平后各种物质的化学计量数从左至右依次为( )
A.1, 3, 14, 2, 1(1/2), 17 B.2, 6, 28, 4, 3, 14
C.1, 6, 14, 2, 3, 7 D.2, 3, 28, 4, 1(1/2),14
8.将反应式:2MnO4‑+10Fe2++16H+ 2Mn2++10Fe3++8H2O设计成原电池,电池的符号是( )
2Mn2++10Fe3++8H2O设计成原电池,电池的符号是( )
A.(-)Pt|Fe2+, Fe3+ || Mn2+, MnO4-, H+|Pt(+)
B.(-) Pt|MnO4-,Mn2+, H+ || Fe2+, Fe3+|Pt(+)
C.(-)Fe|Fe2+, Fe3+ || Mn2+、MnO4‑, H+|Mn(+)
D.(-)Mn|MnO4-, Mn2+、H+ || Fe2+、Fe3+|Fe(+)
9.在[Co(en)(C2O4)2]配离子中,中心离子的配位数为( )
A.3 B.4 C.5 D.6
10.下列配合物中,中心离子以d2SP3杂化的是( )
A.[Ni(CN)4]2- B.[Zn(CN)4]2-
C.[Co(NH)6]3+ D.[SbF5]2-
11.在常温下,Cl2、Br2、I2与NaOH作用正确的是( )
A.Br2生成NaBr, NaBrO3 B.Cl2生成NaCl, NaClO
C.I2成NaI,NaIO D.Cl2生成NaCl, NaClO3
12.气态SO2分子的几何构型是( )
A.线性 B.平面三角形 C.角型 D.三角锥
二、填空题
1.同离子效应使难溶电解质的溶解度________;盐效应使难溶电解质的溶解度 ;后一种效应较前一种效应_________得多。
2.写出锌电极与饱和甘汞电极组成的(φ0Zn2+/Zn=-0.76V ,φ0Hg2Cl2/Hg=0.2415V,)原电池符号 ;正极反应: ;
负极反应: ;电池反应: ;
平衡常数表达式: 。
3.[Ni(en)2]·Cl2命名为________________。
4.三氯·三硝基合钴(III)酸钾的化学式为: 。
5.电解食盐水时,在阴、阳电极上产生的是 ___________和________。
6.在硫的含氧酸盐“过二硫酸盐,硫代硫酸盐,连多硫酸盐和硫酸盐”中,氧化能力最强的是 ________________,而还原能力最强的是 _______________。
7.用化学方程式写出两种鉴定Fe3+ 的方法:
(1) _____________________________________;
(2) _____________________________________。
8.在所有金属中,密度最大的是 ______________;而展性最好的是 _____________。
三、简答题
1.单斜硫和臭氧都是单质,它们的△fHo是否等于零?说明理由。
2.用4个量子数写出下列各族元素的价电子构型通式。
A.惰性气体 B.第IB族元素 C.第VA族元素
3.用杂化轨道理论或价电子对互斥理论判断以下分子中心原子的杂化类型和空间几何构型。
A.NH4+ B.PCl5 C.BF3 D.SO3
4.根据电极电势解释下列现象:
(1)金属铁能量换Cu2+,而FeCl3又能溶解铜板。
(提示:∵φ0Cu2+/Cu>φ0Fe2+/Fe,而φ0Fe3+/Fe2+>φ0Cu2+/Cu)
(2)SnCl2溶液贮存易失去还原性。
5.根据杂化轨道理论,确定下列配合物的杂化类型、分子构型和轨道类型。
| [Fe(H2O)6]2+ | [Ag(Cl)2]- | [Fe(CN)6]3- | |
| 杂化类型 | SP3d2 | ||
| 分子构型 | 正八面体 | ||
| 内外轨 | 外轨型 |
6.用化学方程式写出两种消除Pb2+ 污染的方法。
四、计算题
1.已知ZnS的Ksp=1.2×10-23,H2S的Ka1=5.7×10-8,Ka2=1.2×10-15,在0.10mol·dm-3ZnSO4的酸性溶液中,通入H2S至饱和,欲使ZnS产生沉淀,[H+]最高不能超过多少?
2.有A、B、C、D、四个反应,在298K时,它们的△rHo m和△rSo m为别为:
| △rHo m (KJ·mol-1) | △rSo m (J·mol-1·K-1) | |
| A | 10.5 | 30.0 |
| B | 1.80 | -113 |
| C | -126 | 84.0 |
| D | -11.7 | -105 |
计算说明:1)在标准状态下,哪些反应能自发进行?
2)某余反应在什么温度时可变为自发进行?
3.根据下面电势图(在酸性介质中):

(1)写出能发生歧化反应的反应方程式;
(2)计算该反应的△rG0;
(3)计算该反应在298K时的平衡常数K。
4.已知 : K稳[Ag(CN)2]-=1.26×1021 K稳[Ag(S2O3)2]3-=2.88×1013
试计算下列反应[Ag(S2O3)2]3-+2CN - = [Ag(CN)2]-+2S2O 的K,并根据平衡常数判断反应进行的方向和程度。
的K,并根据平衡常数判断反应进行的方向和程度。
有机化学部分
一、单选题
1.下列化合物中碳原子杂化轨道为sp2的有( )
A.CH3CH3 B. C.C6H6 D.CH≡CH
C.C6H6 D.CH≡CH
2.下列化合物酸性最强的是( )
A.氟乙酸 B.氯乙酸 C.溴乙酸 D.碘乙酸
二、填空题
1.能区别五个碳以下的伯、仲、叔醇的试剂为 。
2.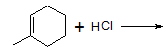 ______________________________。
______________________________。
三、简答题
1.用简单化学方法鉴别甲苯、甲基环己烷、乙醛、乙酸
| 试剂 | 甲苯 | 甲基环己烷 | 乙醛 | 乙酸 |
2.以丙烯为原料(其它试剂任选)合成丙醇。
四、推导题
1.分子式为C3H7Br的A,与KOH-乙醇溶液共热得B分子式为C3H6,如使B与HBr作用,则得到A的异构体C,推断A、B、C的结构式。
教法技能(化学教学)
一、单选题
1.新化学课程的三维目标是指:①知识技能目标,②认知目标,③过程与方法,④培养科学探究能力,⑤情感、态度与价值观( )
A. ①②⑤ B. ①③⑤
C. ②③④ D. ②③⑤
2.现代学习方式的基本特征是:①主动性,②自觉性,③独立性,④独特性,⑤体验性,⑥问题性,⑦参与性( )
A.①②③④⑤ B. ①②③⑤⑥
C.①③④⑤⑥ D. ①④⑤⑥⑦
3.化学教学的主要教学原则是:①目的性,②趣味性,③科学性,④体验性,⑤开放性,⑥循序渐进( )
A. ①②③ B. ④⑤⑥
C. ②③⑥ D. ①③⑥
二、填空题
1.高师院校着重培养师范生的三个能力是指: 。
2.单元教学设计包括的主要内容是: 。
3.纸笔测验评价中对命制试卷的主要要求是: 。
4.初中化学新课程包含: 等五个一级主要内容。
5.科学探究的主要步骤是:
三、简答与分析题
1.教师的专业素质由几个方面组成,你在教学中如何体现?
2.如果你到某中学应聘,校长要求你上一节“酸的分类及性质”课,你需要做那些准备工作?
四、教学设计题
1. 以下课题是高中化学必修教材(化学2)第四章的一个教学课题:“二氧化碳的性质”,请你完成下面的教学设计任务:
(1)拟定教学目标;
(2)分析重、难点;
(3)设计出主要的教学流程或教学要点。
2.试写出以上课题的说课案。
参考书目:
1.《义务教育化学课程标准(2011年版)》,中华人民共和国教育部制订,北京师范大学出版社出版。
2.义务教育课程标准实验教科书。
3.高等师范院校化学专业(专科)相关教材。